Terapia celular reduz tempo de regeneração do fígado
22 de setembro de 2013 | Autor: antonini
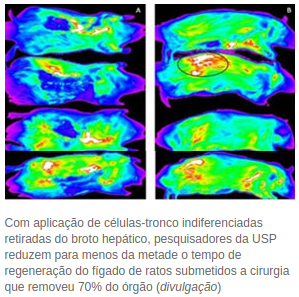
Com aplicação de células-tronco indiferenciadas retiradas do broto
hepático, pesquisadores da USP reduzem para menos da metade o tempo de
regeneração do fígado de ratos submetidos a cirurgia que removeu 70% do
órgão
Uma terapia celular desenvolvida por pesquisadores da Universidade de
São Paulo (USP) reduziu para menos da metade o tempo de regeneração do
fígado de ratos submetidos a uma cirurgia que removeu 70% do órgão.
O objetivo imediato é testar a eficácia do método no tratamento de
cirrose hepática induzida em animais. Futuramente, os cientistas
pretendem avaliar a possibilidade de adaptar o tratamento para humanos.
As células-tronco usadas no estudo foram obtidas do broto hepático de
embriões de ratos com 12 dias e meio de gestação, explicou Maria
Angélica Miglino, professora da Faculdade de Medicina Veterinária e
Zootecnia (FMVZ) da USP e coordenadora da pesquisa financiada pela
FAPESP .
Nos mamíferos, logo no início da gestação surge uma estrutura conhecida
como intestino primitivo, a partir da qual se formam os brotos que darão
origem a todos os órgãos da cavidade abdominal, como o fígado, o
pâncreas, a bexiga e as alças intestinais, disse Miglino.
As células-tronco do broto hepático têm tendência natural para se
transformar em hepatócitos e, por conta disso, seriam teoricamente mais
seguras e eficientes para uso no tratamento regenerativo do fígado
quando comparadas a qualquer outro tipo de célula-tronco.
Essas células têm potencial para formar um fígado. Nossos objetivos
eram descobrir quando elas são formadas, qual seria o melhor momento
para retirá-las do embrião, cultivá-las in vitro e usá-las para tratar
cirrose induzida em ratos, contou Miglino.
Durante o mestrado de Amanda Olivotti, realizado na FMVZ com orientação
da professora Rose Eli Grassi Rici, os pesquisadores identificaram o
momento ideal da gestação para obtenção das células-tronco, realizaram o
cultivo, a caracterização morfológica e as análises histológicas.
As células mostraram grande capacidade proliferativa, mantendo-se
pluripotentes principalmente na metade do 12º dia após a fecundação. Não
apresentaram marcadores de transformação neoplásica ou de erros
genéticos, contou Olivotti.
O passo seguinte, realizado já no doutorado de Olivotti, foi induzir o
quadro de insuficiência hepática nos animais para testar o poder
regenerativo da terapia.
No primeiro grupo de roedores foi retirado 70% do fígado. Isso causa
déficit metabólico e leva a uma insuficiência equivalente a dos casos de
perda do órgão por trauma. Também simula a condição de crianças que
nascem com o fígado atrofiado, disse Durvanei Augusto Maria,
pesquisador do Laboratório de Bioquímica e Biofísica do Instituto
Butantan e coorientador do trabalho.
Em um segundo modelo animal, a cirrose foi induzida pela administração
de medicamentos que causam fibrose nas células do fígado, levando a um
quadro semelhante ao provocado pelo consumo excessivo de álcool ou pela
inflamação crônica resultante de doenças como hepatite.
Vias de administração
Os pesquisadores testaram quatro diferentes vias de administração da
terapia nos ratos hepatectomizados. As células-tronco foram marcadas com
uma substância fluorescente para que seu deslocamento pelo corpo pudesse
ser monitorado por meio de exames de ultrassom, raios X e tomografia de
emissão de pósitrons (PET).
A primeira via avaliada foi a endovenosa, na qual as células eram
introduzidas no organismo dos ratos por meio da veia peniana. Em um
segundo grupo de roedores, as células foram injetadas no peritônio,
membrana que reveste os órgãos da cavidade abdominal.
A terceira via testada foi a endotraqueal, que consistia em passar uma
sonda no interior da traqueia e levar as células até o pulmão. Alguns
pacientes com cirrose desenvolvem síndrome respiratória e essa seria uma
via alternativa para promover primeiro melhora no pulmão e, em segunda
instância, no fígado, explicou Augusto Maria.
Por último foi avaliada a via oroenteral, na qual uma sonda era
introduzida pela cavidade oral, passava pela faringe, esôfago, estômago
e aplicava as células-tronco no duodeno. Por essa via, segundo Olivotti,
as células chegaram em maior número ao fígado e se mantiveram constantes
no órgão por mais tempo.
Obtivemos os melhores resultados pela via oroenteral por causa do ducto
hepático, canal que une o duodeno e o fígado e serve normalmente para a
passagem da bile. Essa via, até hoje, ninguém havia testado, disse
Miglino.
Segundo Augusto Maria, a intenção é avaliar uma quinta via de
administração, mais direta, porém de maior risco: a artéria hepática.
Do ponto de vista cirúrgico, é mais fácil passar uma sonda do que mexer
com uma artéria. Mas pretendemos avaliar também essa via, pois a ideia é
desenvolver um modelo de tratamento que tenha reprodutibilidade em
humanos, disse.
Os animais foram acompanhados por 21 dias. Após esse período, as
células-tronco se mostraram viáveis em todas as vias de administração,
com maior ou menor eficácia em termos de regeneração do fígado.
Um fígado leva em média 25 dias em modelos experimentais para se
regenerar após a hepatectomia. Com a aplicação de uma única dose de
células-tronco indiferenciadas do broto hepático nos animais submetidos
à hepatectomia, a média foi reduzida para dez dias, mostrando ser um
sistema altamente eficaz, disse Olivotti.
Embora o fígado dos animais tenha voltado ao volume original, sua
funcionalidade ainda não foi avaliada pelos pesquisadores. Essas
análises serão feitas até o fim do doutorado, mas os resultados in vitro
indicam que o órgão manteve sua capacidade de metabolização, disse
Olivotti.
O modelo piloto de cirrose induzida por medicamentos precisou ser
revisto, uma vez que a droga usada na primeira tentativa a
dimetilnitrosamina (DMN) mostrou-se agressiva demais e poucos animais
sobreviveram ao experimento.
Iniciamos um novo protocolo de indução com tiocetamida (TAA), que é
menos agressiva, mas o processo de desenvolvimento de cirrose leva mais
tempo para acontecer, disse Olivotti.
No momento, os pesquisadores também fazem um novo modelo de indução por
hepatectomia no qual 90% do fígado é removido cirurgicamente. Este
protocolo tem de ser mais invasivo para podermos monitorar por mais
tempo o processo de regeneração do fígado, explicou.
Aplicação clínica
Embora a estratégia tenha se mostrado promissora, ainda há muitos
obstáculos a serem vencidos até que a terapia possa ser testada em
humanos. O primeiro deles é descobrir uma forma viável para obter as
células do broto hepático.
Ainda que a lei permitisse, não podemos usar embriões remanescentes de
tratamentos de reprodução assistida, pois nessa fase de desenvolvimento
o intestino primitivo ainda não está formado, disse Miglino.
Embora seja tecnicamente possível usar células de fetos que sofreram
aborto espontâneo ou provocado, haveria muitas questões éticas e legais
envolvidas.
Uma possibilidade seria formar um banco de células de primatas
adaptadas a formar fígado humano. Mas precisamos investigar ainda se o
transplante entre espécies diferentes seria viável, disse Miglino.
Para Augusto Maria, ainda serão necessários estudos de longa duração com
animais para que todos os riscos dessa terapia sejam avaliados. É
possível que a aplicação das células induza a formação de trombos e crie
áreas infartadas. Pode ainda formar um tumor ou induzir doenças
autoimunes, ponderou.
Os estudos de longa duração, acrescentou, também são necessários para
entender se as células-tronco estimulam o tecido agredido a se regenerar
ou se são elas próprias que se proliferam dentro do órgão.
Uma possível estratégia seria induzir cirrose em porcos para avaliar os
efeitos da terapia celular. O fígado suíno é o que mais se assemelha ao
humano, disse Augusto Maria.
Os resultados preliminares estão agora sendo enviados para publicação. A
pesquisa está vinculada ao Projeto TemáticoO enigma vitelino, também
coordenado por Miglino.
Leia o texto original
aqui


